Biyokimya, bitki, hayvan ve mikroorganizma biçimindeki bütün canlıların yapısında yer alan kimyasal maddeleri ve canlının yaşamı boyunca sürüp giden kimyasal süreçleri inceleyen bilim dalıdır.
Biyokimyanın amacı her şeyden önce, hücre nin temel bileşenleri olan protein, karbonhidrat, lipit gibi organik bileşiklerin ve yaşamsal önem taşıyan kimyasal tepkimelerde en büyük rolü oynayan DNA nükleik asitlerin, vitaminlerin ve hormonların yapısal ve nicel çözümlemesini yapmaktır. Canlılardaki protein bileşimi, besinlerin enerjiye dönüşmesi, kalıtsal özelliklerin kimyasal mekanizmalarla iletilmesi gibi yaşam süreçlerinin araştırılması da yine biyokimyanın ilgi alanına girer.
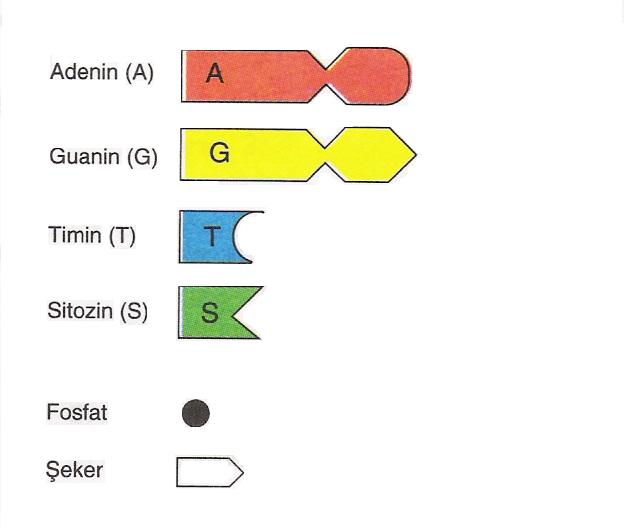
NÜKLEOTİTLER: Nükleotitler çok çeşitli biyokimyasal süreçlerde yer alan, düşük moleküler ağırlıklı hücre içi moleküllerdir. Bilinen en önemli özellikleri pürin ve pirimidin nükleotitle-rinin hücresel DNA ve RNA moleküllerini oluşturmalarıdır. Pürin ribonükleotitlerinin yine yaşam aktivitesi açısından büyük önem taşıyan yüksek enerjili ATP moleküllerinin kaynağı olduğunu da belirtmek gerekir. Adenin nükleotidi aynı zamanda Önemli koenzimlerin yapısında da yer alır. Pirimidin nükleotitleriyse nükleikasitlerin monomer üniteleri olmalarının yanı sıra karbonhidrat metabolizmasında ve lipidbiyosentezlerindeyer alan yüksek enerjili ara moleküller oluştururlar. Nük-leozitler, pürin ya da primidin bazlarının bir şeker molekülüyle friboz ya da deoksiriboz) birleşmesiyle oluşan yapıdır. Örneğin adenozin nükleozidi, adenin ve D-ribozun birleşmesinden oluşur. Nükleotitlerse nükleozitîerin şeker yapısındaki bir ya da daha fazla serbest hidroksil grubunun fosforillenmesiyle oluşan yapılardır. Örneğin adenozin monofosfat (AMP) nükleotidi adenozin ve
fosfattan oluşur.Pürin ve pirimidinlerin doğada oluşan serbest baz biçimleri nükleozit ve nükleotit olarak bulunan biçimlerinden daha fazla oranda bulunurlar.
[img]
[/img]
PROTEİNLER: Serum proteinleri albumin ve globulinlerden oluşmuştur. Plazmada ise bunlara ek olarak fibrinojen vardır. Albumin homojen bir protein molekülüdür. Fakat globulinler en az 4 değişik protein moleküllerinden oluşmuştur. Serum proteinlerinin elektroforeziyle bu globulinler ayrılır ve 2 globulinler diye adlandırılır. Aşağıdaki resimler bir elektroforez grafiğini ve fotoğrafım göstermektedir. Serumun total protein miktarı % 6-8 g arasındadır. Bunun % 3.5-5 g’ı albumin, kalanı globulinlerdir.Serum proteinlerindeki patolojik durumlar genellikle albumin azalması ya da globulinlerin artışı biçimindedir. Açlık, proteinden fakir beslenmeler, karaciğer sirozu, hipotiroidi, alkol alınması, nefrotik sendrom, bakteri entoksikasyonları, kronik infeksiyonlar, habis tümörler gibi olaylarda serum albumin değerleri azalmaktadır. CXı globulin, total proteinin % 1-5′ini oluşturmaktadır. Kronik infeksiyonlarda, romatoid artritte, akut ve kronik nefritlerde düzeyleri artmaktadır. (X 2-globulin, total proteinin % 8-13′ûnü oluşturmaktadır. Akut infeksiyonların ilk devresinde, kronik infeksiyonlarda, sistemik lupus eritamatosus, romatoid artritte, viral hepatitte, karaciğer nekrozunda, sirozda, alfa tip miyelomda artışlar olmaktadır. *U -globulin, total proteinin % 11-17’sini oluşturmaktadır. En belirgin artışlar sirozda olmaktadır. Ayrıca bazı lipid metabolizması bozukluklarında, nefrozda ve beta tip miyelomada dapglobulinler artmaktadır. 2f globulin, total proteinin % 15-25′ini oluşturmaktadır. Bu globulin fraksiyonu immunglobulinleri içermektedir. Multiple miyelomada, bazı lösemi türlerinde, sirozda, aşırı duyarlılık tepkilerinde kolloj en hastalıklarında artmaktadır.
SODYUM: “Sodyum” (Na) hücre dışındaki katyonlar arasında en çok bulunan madendir. Sodyum vücudun asit-baz dengesinin ayarlanmasında etkili olduğu gibi, organizmadaki ozmotik basıncın oluşmasına da katkıda bulunarak, vücudun su tutmasını sağlamaktadır. Sodyum aynı zamanda kas hücrelerinin kasılma işlevinde, hücre içi ile hücrelerarası ortam arasındaki su ve elektrolit alışverişinde görev alan bir madendir. Hergün besinlerle ahnan sodyumun miktarı 3 g kadardır. Sodyumun vücuttan atılmasını sağlayan en önemli iki mekanizma ise terleme ve idrardır. Bu nedenlerle sıcakta terlemiş olan kimselerin duşla birlikte bir miktar da tuz almaları gereklidir.Organizmadaki tuz fazlalığı da tuz azlığı da olumsuz sonuçlar yaratmaktadır, örneğin fazla tuzlu yiyen kimselerde kandaki tuz miktarı artmaktadır. Bu ise belli bir tansiyon yükselmesine neden olmaktadır.Bilindiği gibi tansiyon yüksekliği ise damar sertliği ile yakından ilgilidir. Vücutta sodyum azalması kusma, kas güçsüzlüğü ve ağrıları, bilinç bulanıklığı ve solunum yetmezliği belirtilerine yol açabilmektedir. Addison hastalığında kanda sodyum azlığı gelişir. Müzmin böbrek yetmezliğinin başlangıç dönemlerinde de hasta idrar yoluyla çok sodyum kaybettiği için sodyum yetmezliğine (hiponatremi) düşebilir.
Aşağıdaki tabloda bazı yiyeceklerin 100 gramında
Yiyecek Sodyum mg. Potasyum mg.
Sofra tuzu 38750 4
Baking powder 10000 150
Salamura zeytin 1500-5500 70-130
Dereotu 1000-1500 200-250
Tuzlu tereyağı 1000 20-25
Peynir 600-800 90-100
Bisküvi-Çörek 1000-1500 125-150
Ekmek 500-600 125-150
Beyin 125-150 200-250
Böbrek 150-175 200-225
Kuzu eti 75 300
Sığır eti 70 350-375
Kuru baklagil 25 800-1200
Çekilmiş kahve 75 32500
Maydanoz 50 750
Patates 5 425
Ispanak 75 680
Marul 30 800
Domates 3 250
Havuç 50 350
Portakal 2 200
Muz 2 375
Lahana 25 250
Patlıcan 3 220
Elma 2 100
bulunan sodyum ve potasyum miktarları verilmiştir.Hücre dışı sıvıların en önemli katyonu sodyumdur. Genel olarak klorür ve bikarbonat iyonları ile birleşmiş durumda bulunurlar ve böylece ortamın asit-baz dengesini ayarlarlar. Sodyum aynı zamanda vücut sıvılarının ozmotik baskısını da sağlar ve böylece aşırı su yitimini önler. Vücudun beslenme alışkanlığına göre aldığı günlük tuz oranının % 90-95′i yeniden idrar yoluyla atılır. Alınan tuzun niceliğiyle diyastolik kan basıncı arasında doğru orantılı bir ilişki olduğu bilinmektedir. Böylece aşırı ölçüde sodyum klorür (sofra tuzu) alınması hipertansiyona neden olur ya da daha önceden varsa artırır.
KALSİYUM: Organizmada öteki zorunlu minerallere oranla en fazla kalsiyum bulunur. 70 kg’lık bir vücudun 1.2 kg’ı kalsiyumdur. Bu rakamın % 99′undan fazlasını kemikler ve dişler oluşturur. Kalsiyumun kemiklerin yapısında yer alması kadar bazı hücresel etkinliklerdeki rolü de yaşam açısından önemlidir. Sinir ve kas fonksiyonları, hormonal etki mekanizması, kanın pıhtılaşması hücresel hareketlilik ve benzeri birçok önemli olayda kalsiyumun vazgeçilmez görevleri vardır.Kalsiyum duodenum veincebağırsaktan kalsiyıım bağlayıcı proteinin (calmodulin) yardımıyla emilir. ” Dışarı atılımı, kandaki düzeyi 7 mg/dl’nin üzerine çıktığında böbrekler aracılığıyla olur. Kalsiyum eksikliğinde tetani ve buna bağlı olarak kas ve sinir bozuklukları görülür.
GLİKOZ: Normal kişilerde açlık kan glikoz düzeyi % 70^110 mg arasında değişmektedir. Açlık kanında bu normal değerlerin üzerindeki kan şekeri değerleri hiperglisemi, altındaki değerler ise hipoglisemi diye adlandırılmaktadır. Kandaki glikoz düzeyi % 170 mg’ın üzerine çıkarsa böbrekler tarafından glikozun hepsi geri emile-mez ve idrara glikoz çıkmaya başlar. Hiperglisemi en sık olarak şeker hastalığında [Diabetes mel-lîtus] görülmektedir. Genellikle insülin hormonunun pankreas bezinden yetersiz salgılanmasına bağlı olan bu hastalıkta, organizmada karbonhidratlar gereği kadar kullanılamazlar ve kanda artarak hiperglisemi oluştururlar. Bunların dışında tiroit bezinin fazla çalışmasında (hipertiroidi), böbreküstü bezinin fazla çalışmasında (Cushing sendromu), aşırı adrenalin salgılanmasında, hipofiz bezinin fazla çalışmasında (akromegali) ve bazı karaciğer hastalıklarında hiperglisemi oluşur, yani kan glikoz düzeyi artar. Buna karşın, pankreastan aşırı insülin hormonu salgılanmasını gerektiren patolojik durumlarda, tiroit bezinin az çalıştığı durumlarda (hipotiroidi), böbreküstü bezinin yetersizliğinde [Addison hastalığı) ve hipofiz bezinin yeteri kadar etkin olmadığı durumlarda kan glikoz düzeyi azalır, yani hipoglisemi oluşur
[img]
[/img]
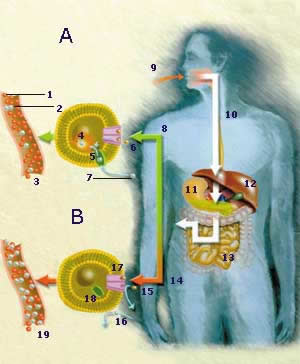
PORFİRİNLER: Dört tane pirol halkasının metilen köprüleriyle birleşerek oluşturdukları halkalı yapılardır. Örneğin hemoglobin yapısında yer alan demir iyonu ile birleşmiş porfirin hem, ve klorofilin yapısında yer alan magnezyum iyonu içeren porfirinler gibi.Doğada proteinlerle birleşerek, önemli biyolojik süreçlerde yer alan metalloporfirinlerden bazıları şunlardır: A] Hemoglobinler: “GIobin”e bağlanmış demirli porfirindir. Kandaki oksijen taşınmasını sağlayan yapılardır. B) Myoglobinler: Omurgalı ve omurgasız canlıların kas hücrelerinde oluşan solunum pigmentleridir. Myoglobin, hemoglobinin bir alt ünitesine benzer yapılı moleküldür. G) Sitokromlar: Oksitlenmeredüklenme reaksiyonlarında elektron taşıyıcı bileşiklerdir. D] Kata-lazlar: Demir içeren porfirinli enzimlerdir. Fizyolojik koşullar altmda, yetişkin insanda bir saatte 100-200 milyon eritrosit parçalanır. Bu duruma göre 70 kg’lık normal bir insanda günde yaklaşık 6 gram hemoglobin ortaya çıkar. Hemoglobin molekülü parçalandığında protein bölümü ya bütün olarak globin biçiminde ya da aminoasit-lerine ayrılarak yeniden kullanıma gider. “Hem” molekülündeki demir de depo havuzlara gider. “Hem” molekülünün demirsiz porfirin bölümü de karaciğer, dalak ve kemik iliği hücreleri tarafından parçalanırlar. Sonuçta biluribin oluşur. Bihıribin de karaciğerde daha ileri düzeyde metabolizmaya uğrar. Biluribinler aktif taşınma mekanizmasıyla safraya da taşınırlar. Burada safra pigmentlerinin oluşumuna katılırlar. Biluri-binlerin bir bölümü de bağırsak florasında urobilinojenlere dönüşürler
[img]

[/img]

